Давно ничего не писала про органы:) когда-то я уже просто и доступно рассказала про нашего маленького помощника – поджелудочную железу и зачем нам печень. Сейчас я расскажу немного о том что такое желчный пузырь, где он находится и зачем вообще знать о его существовании (коротко). А подробней остановимся на особом меню для него. Что любит желчный пузырь, что съесть, чтобы сделать ему приятно и поддерживать его здоровье.
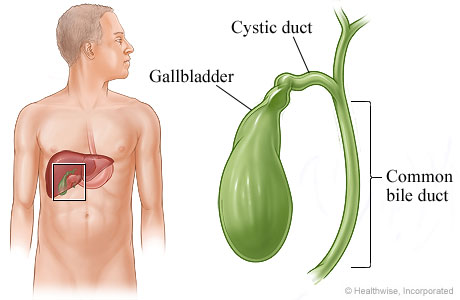
Как видно на схеме, желчный пузырь – небольшой зеленый «мешочек” размером с маленькое куриное яйцо, который спрятан снизу, в полости между долями печени. В нем накапливается желчь. Если объяснять очень просто: печень вырабатывает желчь, постоянно, она необходима для нормального пищеварения. Но так как в самом процессе переваривания еды она нужна лишь периодически, в организме есть для нее особый резервуар – желчный пузырь, который дозирует выброс жидкости с помощью желчных протоков и «клапанов”, так происходит, когда в желудке появляется еды.
Желчь – особая секреция, которую вырабатывают клетки печени. Помогает процессу пищеварения, повышает активность ферментов поджелудочной железы и кишечных ферментов, отвечает за распад и всасывание жиров, способна прекращать действие желудочного сока, обладает бактерицидными свойствами. В сутки организм производит от 1 до 1,8 л желчи.
Заболевания связанные с желчным пузырем чреваты серьезными последствиями. Злоупотребляя продуктами стимулирующими желчевыделение, в организме могут образоваться желчные камни (отсюда нарушение жирового обмена и увеличение массы тела). Или наоборот, продукты дающие слабый эффект сокращения мышц и выделения желчи образуют ее недостаток (отсюда и отсутствие в организме важнейших жирных кислот, жиров и витаминов, а также патологии нижних отделов кишечника). И чтобы не было проблем с жировым обменом, иногда стоит делать приятно желчному пузырю и употреблять его любимые продукты, поддерживающие его здоровье и нормализующие важные его функции.
Продукты, стимулирующие сильное желчевыделение
Мясо, яичные желтки, молоко и молочные продукты (кроме кисломолочных), жиры (растительные масла, продукты, богатые эфирными маслами, жирная рыба и т.п.). Эти продукты стоит свести к минимум особенно в том случае, если у вас наблюдаются заболевания печени. Если вы абсолютно здоровы, можно устраивать себе разгрузочные дни. В таком случае на день, кроме вышеперечисленных продуктов, стоит исключить кислые ягоды и фрукты, острые маринованные овощи и холодные напитки.

Что любит желчный пузырь
Чтобы сделать приятное вашему желчному пузырю и наладить его работу, стоит чаще употреблять отварные или запеченные продукты, первые блюда, разваренные полувязкие каши и бобовые, пить теплые напитки. А при хорошем здоровье и вовсе достаточно лишь чаще употреблять рис, овсяную кашу, есть больше фруктов и овощей, пить овощные фреши (морковь, свекла, можно с добавлением спелых сладких яблок) и смузи (рецепты овощных смузи), и, конечно же, заниматься спортом.
Желчнокаменная болезнь (ЖКБ) в последние несколько десятилетий стала одним из наиболее часто регистрируемых органических заболеваний человека, достигнув распространенности в индустриально развитых странах в пределах 10-15% (в популяции взрослых). Это объясняет большое количество плановых и экстренных хирургических вмешательств по поводу ЖКБ во всем мире . Только в США ежегодно выявляют около 1 млн новых случаев ЖКБ, затраты на лечение этого заболевания превышают 6 млрд долларов в год . В России ежегодно выполняют около 200 тыс. холецистэктомий, в основном лапароскопическим путем .
В среднем только у 20% пациентов с ЖКБ отмечается симптомное течение, к которому относится и классическая желчная колика . При таком течении ЖКБ хирургическое вмешательство позволяет достичь купирования симптоматики у 53,0-81,5% пациентов , уменьшить выраженность диспепсии и абдоминальной боли в 56% и 72% случаев соответственно . К сожалению, весьма существенная часть пациентов (около 40%) не отмечает разрешения абдоминальной боли и симптомов диспепсии после холецистэктомии, более того, в 12,0-38,6% от всех случаев холецистэктомии мучительные симптомы впервые появляются после оперативного лечения . В целом абдоминальная боль и диспепсия после холецистэктомии регистрируются в широких частотных рамках (от 5,6% до 57,3%), что определяется различиями в дизайне исследований . Таким образом, до половины пациентов в разные сроки от момента холецистэктомии предъявляют жалобы на боли в животе, симптомы желудочной и кишечной диспепсии, которые могут иметь как органические, так и функциональные причины .
ПОСТХОЛЕЦИСТЭКТОМИЧЕСКИЙ СИНДРОМ
Дефиниция и краткий экскурс в историю
Следует отметить, что постхолецистэктомический синдром (ПХЭС) только на первый взгляд является простой проблемой, сложности понимания этого синдрома начинаются уже с его определения .
Первые работы, где так или иначе описываются патологические состояния после удаления желчного пузыря, появились в зарубежной литературе в конце 30-х годов прошлого века . Наиболее важной и интересной остается первая серия наблюдений, представленная J. Hellstrom (с учетом данных, полученных K. K. Nygaard) в 1938 г. Она насчитывала 141 пациента после удаления желчного пузыря, 30% от общей выборки имели спастические боли в животе, аналогичные тем, что были до хирургического вмешательства. Только у 9 пациентов удалось выявить холедохолитиаз, еще реже диагностировался острый панкреатит. В большинстве случаев причины болей объяснить не удалось, в связи с чем выявленные боли автор назвал «постхолецистэктомической коликой» .
Следующая крупнейшая серия наблюдений была представлена H. Doubilet в устном докладе на заседании хирургической секции Нью-Йоркской академии медицины в апреле 1943 г. и подробно изложена в последующей обзорной работе R. Colp . Цитируемая серия насчитывала 253 пациента после холецистэктомии со сроками наблюдения от 1 года до 7 лет. У 40% пациентов имелись упорные послеоперационные симптомы, зачастую сходные с клиническими проявлениями до холецистэктомии. Именно в этих двух работах впервые встречается термин ПХЭС, в рамках которого авторы объединили комплекс различных расстройств после холецистэктомии. Бóльшая часть постхолецистэктомических расстройств, ввиду отсутствия органических причин (культя пузырного протока, резидуальный холедохолитиаз и т. д.), исследователями тех лет признается функциональными расстройствами, сопровождающимися рецидивными болями по типу колик. Авторы предположили, что базис часто регистрируемых функциональных болей — нарушение моторики спастического типа (дискинезия) сфинктеров билиарного тракта и кишечника, а также пограничные расстройства психики у некоторых больных. Одним из веских оснований для подобного суждения явилась констатация более высокой частоты развития постхолецистэктомических функциональных расстройств у пациентов с потенциально функционирующим желчным пузырем (бескаменный холецистит или калькулезный холецистит без выраженного фиброза стенки желчного пузыря) . Таким образом, авторы впервые в истории изложили четкие представления о возможности формирования постхолецистэктомических расстройств, выделили потенциальные группы признаков, повышающих риск их развития:
-
наличие функциональных причин боли и диспепсии до холецистэктомии;
- пограничные расстройства психики у пациентов до хирургического вмешательства;
-
наличие функционирующего желчного пузыря.
С учетом опыта и знаний, накопленных к настоящему времени , можно полагать, что:
-
функциональные заболевания, проявлявшиеся жалобами на боль и диспепсию до холецистэктомии, могут персистировать или усугубляться после оперативного вмешательства;
- пограничные расстройства психики у пациентов с функциональными заболеваниями ЖКТ встречаются чрезвычайно широко, тесно переплетаясь в общем патогенезе соматоформного заболевания; поэтому пограничные расстройства психики до хирургического вмешательства по поводу ЖКБ (которая может сочетаться, например, с синдромом раздраженного кишечника — СРК) определенно будут сохраняться и после, формируя стойкую или даже прогрессирующую функциональную симптоматику боли и диспепсии;
-
удаление функционирующего желчного пузыря (бескаменный острый холецистит, I стадия ЖКБ с билиарным сладжем, солитарные конкременты у молодых людей) может повышать риск дезадаптивных функциональных расстройств в послеоперационном периоде относительно такового у лиц, прооперированных в иных условиях (нефункционирующий, «отключенный» желчный пузырь и т. п.).
Возвращаясь к первым работам, формировавшим представление о ПХЭС, следует отметить, что гипотеза о спазме сфинктеров билиарного тракта как о причине функциональной боли после холецистэктомии легла в основу эмпирического применения нитратов и атропина для купирования спазма . Ряд простых описательных исследований тех лет позволил разработать показания и даже обсуждать теоретические возможности папиллотомии, опираясь на экспериментальные работы начала прошлого века.
В 1940-1970-е годы термин ПХЭС прочно закрепился и регулярно встречался в научной литературе , к середине 1970-х число таких работ достигло ста . Любопытно, что в одной из первых отечественных работ, реферируемых в международных базах данных , продемонстрировано скептическое отношение к термину ПХЭС и содержится его активная критика. Что еще более интересно, с конца 60-х годов прошлого века число англоязычных статей на тему ПХЭС в наиболее авторитетных международных журналах стремительно падает и к 80-м годам практически сводится к нулю, в то время как в Восточной Европе и СССР количество работ, посвященных ПХЭС, напротив, значительно увеличивается. В 1980-х годах в связи с отказом от термина ПХЭС в авторитетных англоязычных журналах его успешно стали заменять постхолецистэктомической болью , папиллярной дисфункцией и даже, используя терминологию 30-х годов прошлого века, — билиарной дискинезией .
Сегодня очевидно, что сложность изучения и верификации постхолецистэктомических расстройств, схожесть симптоматики при органических изменениях и функциональных нарушениях привели к тому, что термин ПХЭС в странах Запада уже к середине 80-х годов XX века перестал использоваться. В международной практике унифицированного термина ПХЭС до сих пор нет, поскольку невероятно сложно определить точный механизм и первопричину боли и диспепсии, возникающих в разные временны́е отрезки после холецистэктомии. Однако, как это ни парадоксально, термин ПХЭС вошел в МКБ-10 и был чрезвычайно популярен в СССР, а сейчас и в России (как в рутинной практике, так и среди научных работников). Широкое признание этого термина в 1970-1980-е годы в СССР не было случайным, оно объяснялось растущим числом холецистэктомий, объективными трудностями диагностики и недостаточным представлением врачей о возможных последствиях вмешательства — от функциональной дезадаптации билиарного тракта (и даже всей системы пищеварения) до грубых органических изменений .
В России сегодня под ПХЭС понимается множество различных заболеваний и состояний, которые возникают у больных после холецистэктомии и теоретически могут быть связаны с ней . Именно невозможность объединения органических изменений и функциональных расстройств единым диагнозом привела к отказу от этого термина за рубежом, где любые отклонения у пациента после холецистэктомии, теоретически связанные с ней, рассматриваются как «состояние после холецистэктомии» . По клиническим показаниям в группах риска и при наличии маркеров органических изменений осуществляется диагностический поиск причины, в противном случае устанавливается диагноз дисфункции сфинктера Одди согласно Римским критериям III .
Структура постхолецистэктомического синдрома
Объективное представление о структуре нозологий, являющихся причинами боли и диспепсии после холецистэктомии, позволяют сформировать результаты недавних клинических исследований. В одном из них в течение 36 месяцев находились под наблюдением 80 пациентов с симптомами боли и диспепсии после удаления желчного пузыря. Комплексное обследование с использованием биохимических тестов (билирубин и щелочная фосфатаза), трансабдоминального и эндоскопического УЗИ, эндоскопической ретроградной панкреатохолангиографии и манометрии сфинктера Одди позволило авторам точно определить причины боли и диспепсии у больных после холецистэктомии. Помимо функциональных расстройств, они включали в себя широкий спектр органических заболеваний гепатопанкреатобилиарной зоны. У бóльшей части (57,5%) пациентов имелась органическая патология билиопанкреатической зоны (рис.). При этом дисфункция сфинктера Одди и комплекс функциональных небилиарных причин (в том числе СРК) составили достаточно большую долю — 42,5% всех случаев (8,75% и 33,75% соответственно) .
Рис. Причины боли и диспепсии у пациентов с перенесенной холецистэктомией, %. Исследовательский центр гастроэнтерологии и гепатологии, Институт медицины и фармации, Крайова, Румыния (по )
По результатам исследования, проведенного в Великобритании с целью оценки частоты диареи у 100 пациентов, наблюдавшихся после холецистэктомии в течение 6-12 месяцев, у 17% из них этот симптом появился впервые и стал персистирующим только после хирургического вмешательства. В качестве наиболее достоверного фактора риска диареи после холецистэктомии авторы указали молодой возраст (ОШ — 3,4; 95%-й ДИ: 1,16-9,96; р = 0,026) . Безусловно, именно у пациентов молодого и среднего возраста наиболее часто встречаются функциональные расстройства ЖКТ, включая СРК . Одна из причин функциональных нарушений со стороны кишечника после холецистэктомии состоит в мальабсорбции желчных кислот и развитии секреторной диареи за счет избыточного и асинхронного поступления неконцентрированной желчи в просвет кишечной трубки. В основе патофизиологии секреторной диареи лежит и ускоренный пассаж содержимого по тонкой и толстой кишке, сопровождающийся гипермоторикой гладкой мускулатуры кишечника. Гипермоторика и спазм с появлением боли — весьма близкие в патофизиологическом плане состояния. Висцеральная гиперчувствительность, спазм (боль) и диарея формируют СРК-подобную симптоматику у некоторых больных после холецистэктомии. Психосоматический фон у части таких пациентов является фактором риска закрепления симптоматики .
Важно отметить еще одну работу, включавшую 158 пациентов, которым планировалось проведение лапароскопической холецистэктомии. Авторами оценивалось качество жизни и проверялось наличие СРК до и после оперативного лечения с использованием критериев СРК (критерии Маннинга и Римские критерии II) и опросника Gastrointestinal Quality of Life (GQL) соответственно. Как оказалось, у 32 (20,3%) пациентов был СРК до холецистэктомии , т. е. несколько чаще, чем в общей популяции (10-17%) . Наблюдение за пациентами в общей выборке в сроки 6, 12 недель и 2 лет после оперативного лечения показало, что холецистэктомия в целом улучшает качество жизни пациентов в раннем восстановительном периоде после оперативного вмешательства. Так, средний балл GQL через 6 недель после операции значительно увеличился: с 88,8 ± 1,3 до 105,5 ± 1,3 (p < 0,001). Подобная картина сохранялась и через 3 месяца. Однако спустя 2 года после операции авторами отмечено значительное ухудшение качества жизни пациентов: в среднем на 7,6 ± 2,3 балла ниже значений до операции (p = 0,003). Вероятно, это произошло как раз за счет развития у части больных тех или иных отклонений, которые можно обозначить как ПХЭС. Важно, что у лиц, страдавших СРК до холецистэктомии, качество жизни ухудшалось уже к 6-й неделе после операции, вероятно, это происходило за счет усугубления симптоматики СРК. У таких больных наличие каждого симптома Маннинга снижало качество жизни на 5,2 ± 1,3 балла по сравнению с основной группой без СРК (p < 0,001). При использовании более современных Римских критериев II оказалось, что у лиц с СРК качество жизни снижается более выраженно — в среднем на 12 баллов по сравнению с общей группой пациентов .
Не удивительно, что в одном из крупнейших на сегодняшний день исследований, проведенном в клиниках Mayo (Рочестер, Миннесота) и Kaiser Permanente (Сан-Диего, Калифорния) и включавшем 1008 пациентов, перенесших холецистэктомию по поводу ЖКБ, были идентифицированы достоверные факторы отсутствия абдоминальной боли после оперативного вмешательства (p < 0,05) :
-
редкая частота болевых приступов (1 раз в месяц и менее);
- манифестация боли в период за 1 год и менее до холецистэктомии;
-
длительность приступа боли от 30 минут до 24 часов;
-
ночные боли;
-
высокоинтенсивные боли.
Как видно из представленных выше факторов, они отнюдь не соответствуют признакам функциональных расстройств, для которых характерны длительное непрогрессирующее персистирование боли, частые кратковременные приступы или затяжные многодневные периоды боли умеренного характера, граничащей с дискомфортом, отсутствие болей в ночной период времени . Более того, авторы цитируемой выше работы отметили, что риск персистирования боли после холецистэктомии может повышаться у соматизированных пациентов, у лиц с болями внизу живота, рецидивирующим вздутием и другими маркерами СРК.
Таким образом, если у пациента был СРК до операции, то весьма возможно, что он сохранится и даже усугубится после оперативного вмешательства. Именно у такого пациента с высокой вероятностью можно ожидать повторных визитов к хирургу и гастроэнтерологу после операции с персистирующими жалобами на абдоминальную боль и симптомы диспепсии, расстройства стула и ухудшение качества жизни . Экстраполируя эти данные, можно полагать, что холецистэктомия у больных ЖКБ, сочетающейся не только с СРК, но и с другими функциональными расстройствами ЖКТ, может иметь худший прогноз в отношении персистирования боли и диспепсии, чем у пациентов, которые страдают лишь ЖКБ.
Патофизиология постхолецистэктомических расстройств
Исходя из множества органических и функциональных причин боли и диспепсии после холецистэктомии, в патофизиологии постхолецистэктомических расстройств необходимо выделить органические и функциональные причины .
1. Органические причины:
-
боли, диспепсия и прочие симптомы, обусловленные органической патологией, связанной с ЖКБ и/или холецистэктомией (культя пузырного протока, холедохолитиаз, острый билиарный панкреатит, стриктуры холедоха и большого дуоденального сосочка и др.) ;
- клинические проявления другой органической патологии, теоретически не связанной с холецистэктомией (опухоли de novo
органов пищеварения).
2. Функциональные причины:
-
дисфункция (спазм) сфинктера Одди, имевшая место исходно или появившаяся/усугубившаяся после холецистэктомии (так называемый истинный ПХЭС);
- нарушение пищеварения вследствие изменения свойств и выделения желчи, получившее название «билиарная недостаточность». Пусть данный термин пока не является общепринятым, однако дефицит эффектов желчи и асинхронизм ее выделения могут способствовать развитию различных патологических состояний, определяющих клиническую картину постхолецистэктомических расстройств: экзокринной панкреатической недостаточности, дуоденогастрального рефлюкса, синдрома избыточного бактериального роста в тонкой кишке (СИБР) и др. ;
-
другие функциональные нарушения органов пищеварения (СРК, функциональная диспепсия, гастроэзофагеальная рефлюксная болезнь).
Чтобы представить патофизиологию постхолецистэктомических расстройств, следует остановиться на функциях желчного пузыря (выпадающих после холецистэктомии) :
-
эвакуаторная функция обеспечивает выделение желчи в двенадцатиперстную кишку (ДПК) в пищеварительный период;
- концентрационная и резервуарная способствуют накоплению концентрированной желчи, которая обладает наилучшими пищеварительными и бактерицидными эффектами;
-
абсорбционная (поглощение отдельных компонентов желчи) лежит в основе компенсаторной реакции при их избытке;
-
секреторная (секреция слизи железами шеечного отдела) облегчает поступление желчи в желчный пузырь и эвакуацию желчи из него;
-
гормональная функция состоит в секреции антихолецистокинина, оказывающего модулирующее влияние на сфинктер Одди.
-
Сфинктер Одди также выполняет важные функции, связанные с работой желчного пузыря :
-
регулирует отток желчи и панкреатического сока в ДПК;
- предотвращает рефлюкс содержимого ДПК в холедох и главный панкреатический проток;
-
обеспечивает накопление желчи в желчном пузыре в период между приемами пищи (так как способен преодолевать секреторное давление печени);
-
осуществляет синхронную работу с желчным пузырем.
Итак, утрата желчного пузыря с потерей его функций и развитием вследствие этого дисфункции сфинктера Одди приводит к снижению качества и количества оттекающей желчи и панкреатического секрета в ДПК, что не всегда может полноценно компенсироваться работой физиологически сопряженных органов пищеварения. В связи с этим создаются реальные условия для пищеварительной дисфункции. Отчасти патогенез ПХЭС обусловлен выпадением функций желчного пузыря: отсутствие эвакуаторной и концентрационной функций определяет нарушение процессов липолиза в тонкой кишке, ослабление бактерицидных свойств желчи. Непрерывное желчеистечение также может определять дисфункцию пищеварения, способствовать формированию билиарных рефлюксов и развитию гипертонуса сфинктера Одди .
Под влиянием измененной тонкокишечной микробиоты деконъюгируются желчные кислоты с последующим повреждением слизистой оболочки, развитием дуоденита, рефлюкс-гастрита и эзофагита. В ряде случаев дуоденит сопровождается дуоденальной гипертензией и дискинезией ДПК, что способствует персистированию патологических рефлюксов .
Клиническая картина постхолецистэктомического синдрома
Боль после холецистэктомии, являясь главной причиной низкого качества жизни больных, исходит из многогранной патофизиологии постхолецистэктомических расстройств, представленной выше. Основная причина абдоминальной боли — функциональная перестройка сфинктерного аппарата желчных путей после утраты желчного пузыря.
Римским консенсусом III пересмотра хорошо представлена клиника трех типов дисфункции сфинктера Одди после холецистэктомии: билиарного, панкреатического и смешанного . При изолированной дисфункции сфинктера холедоха возникают билиарные боли, локализующиеся в эпигастрии и/или правом подреберье с возможной иррадиацией в спину, правую лопатку. При преимущественном поражении сфинктера главного панкреатического протока типичными являются боли так называемого панкреатического типа, локализующиеся в эпигастрии и левом подреберье, порой иррадиирующие в поясничную область, спину. При спазме общего сфинктера отмечаются сочетанные билиарно-панкреатические боли, часто описываемые как «опоясывающие» .
Тактика ведения и принципы лечения пациентов с постхолецистэктомическим синдромом
Базисом подходов к контролю боли и диспепсии после холецистэктомии служит своевременное и правильное установление их причин. Первоочередной задачей является исключение органической патологии органов пищеварения, которая может служить причиной жалоб, — холедохолитиаза, билиарных стриктур, опухолевых заболеваний билиопанкреатической зоны и др. Наличие подобных изменений, как правило, диктует необходимость хирургического или эндоскопического лечения. При отсутствии органических причин персистирования симптоматики следует думать о функциональном характере боли и диспепсии, особенно если имеется ассоциация с рядом косвенных маркеров функциональных болей :
-
текущие симптомы имели место и до операции, а в послеоперационном периоде появились снова, с той же или даже с большей выраженностью;
- имеется длительное непрогрессирующее течение заболевания;
-
известно о расстройствах психики и/или применении психотропных средств до холецистэктомии;
-
хронические жалобы соответствуют критериям функциональных расстройств органов пищеварения — функциональной диспепсии, дисфункции сфинктера Одди, СРК.
Констатация факта функциональных расстройств органов пищеварения как причины боли и диспепсии после холецистэктомии является показанием к консервативному лечению. Основа выбора лекарственных средств для коррекции функциональных постхолецистэктомических спазмов и диспепсических расстройств эмпирическая, при этом большинство врачей предпочитают комбинированную фармакотерапию с обязательным использованием препаратов спазмолитического действия. Дополнительно могут назначаться средства для коррекции СИБР (кишечные антисептики, пищевые волокна, энтеросорбенты), дуоденогастрального рефлюкса (прокинетики, препараты урсодезоксихолевой кислоты, сорбенты), современные микрокапсулированные препараты панкреатина для коррекции вторичной панкреатической недостаточности и др.
К сожалению, унифицированных схем фармакотерапии ПХЭС не существует, что объясняется частым сочетанием (так называемым перекрестом) различных функциональных расстройств у одного больного, способных чередоваться во времени, а также наличием необязательных, но часто сопутствующих синдромов (СИБР и др.) после холецистэктомии. Следует отметить, что в случае доказанной дисфункции сфинктера Одди, резистентной к адекватному консервативному лечению в течение 3 месяцев, возможно эндоскопическое воздействие (эндоскопические папиллотомия и стентирование холедоха). Остальные случаи функциональных расстройств после холецистэктомии требуют консервативного лечения.
Выбор спазмолитика в рутинной практике также осуществляется эмпирическим путем, так как верифицировать тип моторных нарушений и провести фармакологические пробы с разными препаратами чрезвычайно сложно. Сравнительных контролируемых исследований, оценивающих эффект воздействия разных спазмолитиков на функцию сфинктера Одди, до сих пор не проведено. Ввиду того что из-за комбинации функциональных расстройств у одного и того же больного довольно сложно сепарировать жалобы, обусловленные дисфункцией сфинктера Одди, функциональной диспепсией и дуоденогастральным рефлюксом, СРК и СИБР, практикующими врачами, как правило, выбираются спазмолитики, способные ликвидировать спазм как в билиарном тракте, так и в кишечнике, приоритетно пролонгированного действия и с минимумом нежелательных явлений, что позволяет эффективно и безопасно использовать их долгосрочно.
ЗАКЛЮЧЕНИЕ
Термин «постхолецистэктомический синдром» является крайне неудачным, в современной англоязычной литературе его заменяют «состоянием после холецистэктомии» ввиду широкого спектра органических и функциональных причин, определяющих персистирование основных проявлений — абдоминальной боли и диспепсии.
Риск развития функциональных расстройств после холецистэктомии повышен у лиц с исходными пограничными расстройствами психики, у пациентов молодого возраста с функционирующим желчным пузырем.
Лишь комплексное обследование больных с использованием биохимических тестов, трансабдоминального и эндоскопического УЗИ и/или эндоскопической ретроградной панкреатохолангиографии и манометрии сфинктера Одди позволяет детально определить причину боли и диспепсии у больных после холецистэктомии.
Основа выбора лекарственных средств для коррекции функциональных постхолецистэктомических спазмов и диспепсических расстройств эмпирическая, при этом большинство врачей предпочитают комбинированную фармакотерапию с обязательным использованием препаратов спазмолитического действия. В случае доказанной дисфункции сфинктера Одди, резистентной к адекватному консервативному лечению в течение 3 месяцев, возможны эндоскопические папиллотомия и стентирование холедоха.
А.А. Ильченко
Центральный научно-исследовательский институт гастроэнтерологии, Москва
Диагностика желчнокаменной болезни (ЖКБ) на стадии сформировавшихся желчных камней является причиной высокой оперативной активности при этом заболевании. Несмотря на внедрение в клиническую практику менее инвазивных, по сравнению с полостной холецистэктомией, технологий, у части пациентов возникают так называемые постхолецистэктомические расстройства, обозначаемые как постхолецистэктомический синдром (ПХЭС).
Несмотря на то, что ПХЭС включён в современную классификацию болезней МКБ-10 (шифр К.91.5), точного понимания сути этого синдрома нет и до настоящего времени.
Согласно Римскому консенсусу по функциональным расстройствам органов пищеварения 1999 г. термином «постхолецистэктомический синдром» принято обозначать дисфункцию сфинктера Одди, обусловленную нарушением его сократительной функции, препятствующую нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий. С подобной трактовкой можно было бы согласиться, если бы не существовало тесной анатомо-функциональной взаимосвязи между билиарной системой и другими органами пищеварения. Удаление желчного пузыря – мера исключительно вынужденная, а патология желчного пузыря, приведшая к холецистэктомии, как правило, развивается длительно и практически всегда ассоциирована с патологией других органов пищеварения, в первую очередь, панкреатодуоденальной зоны. Поэтому трудно представить, что утрата желчного пузыря не отразится на течении патологических процессов, развившихся до операции.
Исходя из этого, с практической точки зрения целесообразно рассматривать ПХЭС с позиции учёта всего комплекса патологических состояний, ассоциированных с длительно протекающим холелитиазом. В связи с этим можно выделить следующие основные группы причин развития ПХЭС:
1. Диагностические ошибки, связанные с выявлением патологии, ассоциированной с билиарной системой, которые были допущены на дооперационном этапе и/или во время операции.
2. Технические погрешности и тактические ошибки, допущенные при проведении операции.
3. Функциональные нарушения, развившиеся после удаления желчного пузыря или усугубленные холецистэктомией.
4. Обострение и/или прогрессирование существовавших до операции заболеваний гепатопанкреатодуоденальной зоны.
Первая группа
Функциональные нарушения билиарного тракта – непременный атрибут холелитиаза, обеспечивающие его формирование и прогрессирование. При ЖКБ наиболее главными являются нарушения в скоординированной работе сфинктера Люткенса и сфинктера Одди. Поэтому диагностика билиарных дисфункций и их коррекция до операции способствуют более быстрой адаптации организма к потере функций желчного пузыря. Недооценка функциональных нарушений на дооперационном этапе в раннем послеоперационном периоде может проявиться различными вариантами дисфункций сфинктера Одди (билиарный, панкреатический или смешанный типы).
Структурные изменения билиарного тракта обычно представлены стенозом терминального отдела общего желчного протока или стенозирующим папиллитом, которые формируются вследствие травматизации слизистой оболочки и непосредственно сфинктерного аппарата мигрирующими микролитами или мелкими конкрементами. Выявление этих и других изменений (холангит, холедохолитиаз и другие) до операции приобретает особое значение, так как определяет не только клинические симптомы, но и тактику ведения больного, готовящегося к холецистэктомии.
Оперативное вмешательство является последним диагностическим этапом, поэтому уточнение характера патологических изменений во время операции необходимо провести в максимально полном объёме с использованием современных методов интраоперационной диагностики – интраоперационной холангиографии, прямой холангиоскопии, а в последние годы и интраоперационной сонографии. В результате подобных диагностических ошибок патологические изменения в общем желчном протоке остаются нераспознанными. Так, например, неполноценное исследование желчных протоков без рентгенологического контроля за их состоянием приводит к тому, что в половине случаев остаются незамеченными камни в протоковой системе .
Вторая группа
Эта группа ошибок является основной причиной формирования так называемого «истинного постхолецистэктомического синдрома» и повторных операций на желчных путях, и они подробно изложены в практических руководствах по хирургии.
Третья группа
После холецистэктомии развивается гипертонус сфинктера Одди, и в первый месяц после операции эта патология отмечается у 85,7 % больных . Гипертонус сфинктера Одди клинически сопровождается билиарной гипертензией, холестазом, болями в правом подреберье, а в ряде случаев развивается клиника обострения билиарного панкреатита.
Механизм развития гипертонуса сфинктера Одди связан с выключением регулирующей роли сфинктера Люткенса и мышечной активности желчного пузыря, так как тонус сфинктера Одди рефлекторно понижается во время сокращения желчного пузыря, что обеспечивает скоординированную деятельность всего сфинктерного аппарата желчных путей. Экспериментально установлено уменьшение реакции сфинктера Одди в ответ на холецистокинин после холецистэктомии. Дисфункция сфинктера Одди в виде его гипертонуса после холецистэктомии обычно носит временный характер и проявляется, как правило, на протяжении первых месяцев после операции. Моторная дисфункция сфинктера Одди является одной из причин формирования острой или хронической абдоминальной боли и диспепсического синдрома в послеоперационном периоде. Следует отметить, что качество жизни после холецистэктомии у больных со сниженной до операции сократительной функцией желчного пузыря лучше, чем с сохранённой или повышенной. Известно, например, что у больных с так называемым отключённым желчным пузырем, дилятация общего желчного протока отмечается редко как до операции, так и после неё. Постепенная адаптация приводит к тому, что у таких больных редко развивается и ПХЭС.
Четвертая группа
Хроническая билиарная недостаточность, сопутствующая ЖКБ, сохраняется и после удаления желчного пузыря. Причём эти изменения выявляются у 100 % больных в первые 10 суток после операции и у 81,2 % пациентов не исчезают после холецистэктомии на протяжении длительного времени . Примечательно, что хроническая билиарная недостаточность определяется уже на начальных стадиях ЖКБ. Так, по данным О.В. Делюкиной , у больных с билиарным сладжем в виде взвеси гиперэхогенных частиц она была выявлена в 91,7 %, причём в 50 % лёгкой, а в 41,7 % – средней степени тяжести.
Дефицит желчных кислот после холецистэктомии до определённой степени восполняется за счёт ускорения их энтерогепатической циркуляции. Однако значительное ускорение энтерогепатической циркуляции сопровождается подавлением синтеза желчных кислот, что приводит к дисбалансу соотношения основных её компонентов и нарушению солюбилизирующих свойств желчи.
Удаление желчного пузыря сопровождается перестройкой процессов желчеобразования и желчевыделения. По данным Р.А. Иванченковой , после холецистэктомии увеличивается холерез как за счёт кислотозависимой, так и кислотонезависимой фракций. Увеличение желчевыделения наступает уже через 2 недели после холецистэктомии. Повышение холереза – основная причина холагенной диареи после холецистэктомии.
Среди органов гепатопанкреатодуоденальной зоны удаление желчного пузыря более всего отражается на функции поджелудочной железы. Развитию хронического панкреатита билиарной этиологии способствуют часто встречающиеся функциональные нарушения (дисфункции сфинктерного аппарата желчных путей) или органические заболевания протоковой системы, нарушающие пассаж желчи (сужение, сдавление кистами или увеличенными лимфоузлами, камни с локализацией в терминальном отделе общего желчного протока, воспалительные процессы, особенно с локализацией в его дистальных отделах и др.). В связи с этим обострение хронического панкреатита у больных, перенесших холецистэктомию, встречается достаточно часто. По данным В.А. Зориной с соавт. , обследовавших больных через 4-10 дней после холецистэктомии, у 85 % больных отмечено повышенное содержание в сыворотке крови b1-антитрипсина, причём в 34,7 % случаев показатели превышали норму более чем в 2 раза.
Хронический гастрит является наиболее распространённой патологией органов пищеварения. Считается, что роль его в формировании постхолецистэктомического синдрома невелика и определяется в основном функциональными нарушениями. Хронический гастрит часто ассоциирован с Helicobacter pylori (НР). В связи с этим обсуждается вопрос о необходимости проведения антихеликобактерной терапии у больных, которым предстоит холецистэктомия. Накопленный опыт, свидетельствующий о том, что антихеликобактерная терапия, проведённая, например, перед резекцией желудка, значительно снижает число послеоперационных осложнений, убеждает в такой же необходимости и в связи с предстоящей холецистэктомией.
В необходимости проведения антихеликобактерной терапии убеждают и последние исследования, свидетельствующие о возможной связи хеликобактерной инфекции с билиарной патологией и гепатобилиарным раком, в частности. По данным F. Fukuda и соавт. , обследовавших 19 больных гепатобилиарным раком и 19 больных с доброкачественными заболеваниями гепатобилиарной системы, с помощью ПЦР выявили хеликобактерную ДНК в образцах желчи соответственно в 52,6 % и 15,7 % случаев. Получены первые доказательства о наличии НР в желчи и слизистой оболочке желчного пузыря у людей , а также данные экспериментальных исследований на животных, подтверждающие роль энтерогепатических хеликобактеров (H. bilis, H. hepaticus, H. rodentium) в билиарном литогенезе . Решение вопроса о роли хеликобактеров в этиологии билиарной патологии может значительно изменить подходы к тактике ведения пациентов с заболеваниями желчевыводящих путей, в том числе и к вопросу профилактики постхолецистэктомического синдрома.
Хронический дуоденит и синдром избыточного бактериального роста (СИБР). Холецистэктомия сопровождается снижением бактерицидных свойств желчи, что приводит к избыточному бактериальному росту в двенадцатиперстной кишки. Этому способствует и снижение барьерной функции желудка, обусловленной гипосекрецией соляной кислоты. Хроническая билиарная недостаточность, снижение бактерицидных свойств желчи и присоединившийся СИБР приводят к существенному нарушению пищеварения, что обуславливает развитие соответствующей симптоматики и требует медикаментозной коррекции.
Таким образом, анализируя характер патологических процессов, связанных с холецистэктомией, можно дать следующее определение постхолецистэктомического синдрома: ПХЭС – совокупность функциональных и/или органических изменений, связанных с патологией желчного пузыря или протоковой системы, усугубленных холецистэктомией или развившихся самостоятельно в результате технических погрешностей её выполнения.
Подобное определение нацеливает врача на более тщательное обследование больных перед операцией с целью выявления различной сопутствующей патологии как органов пищеварения, так и других органов и систем, позволяет понять патогенетическую связь между оперативным вмешательством и развившейся клинической симптоматикой после него.
Анализ клинической симптоматики позволил выделить следующие варианты течения ПХЭС:
• диспепсический вариант – с явлениями диспепсии в виде тошноты, ощущения горечи во рту и невыраженным болевым синдромом;
• болевой вариант – с болевым синдромом различной степени выраженности;
• желтушный вариант – периодически субэктеричность кожных покровов и склер с или без болевого синдрома;
• клинически асимптомный вариант – с отсутствием жалоб, с наличием изменений в биохимических показателей крови (повышение уровней ЩФ, билирубина, АсАТ, АлАТ, амилазы) и/или дилатацией ОЖП по данным УЗИ более 6 мм.
Результаты обследования 820 больных с ПХЭС показали, что наиболее часто по сравнению с другими встречается диспепсический вариант (рисунок).
Диагностика
Для диагностики ПХЭС применяют методы, позволяющие выявить функциональные и структурные нарушения билиарного тракта, протекающими как самостоятельно, так и в ассоциации с другими заболеваниями органов пищеварения. В качестве скрининговых используют лабораторные (определение уровней ГГТП, ЩФ, билирубина, АсАТ, АлАТ, амилазы) и инструментальные (УЗИ, ЭГДС) методы диагностики. В качестве дополнительных методов – эндоскопическую ретроградную холангиопанкреатикографию (ЭРХПГ), в т. ч. с манометрией сфинктера Одди, динамическую холесцинтиграфию, магнитно-резонансную холангиографию, эндоскопическую ультрасонографию, этапное хроматическое дуоденальное зондирование и другие методы.
Тщательное обследование больных ПХЭС с использованием высокоинформативных методов диагностики позволяет провести своевременную и адекватную коррекцию анатомо-функциональных нарушений, развившихся после удаления желчного пузыря или усугублённых холецистэктомией.
Лечение
В большинстве случаев консервативное лечение позволяет провести коррекцию основных патофизиологических нарушений при ПХЭС, однако в различные сроки после холецистэктомии могут появиться показания и для оперативного лечения.
Важное значение в раннем послеоперационном периоде имеет лечебное питание. Диетические рекомендации заключаются в частом (до 6 раз в день) и дробном питании. Необходимо ограничение жиров до 60-70 г в сутки. При сохранённой функции поджелудочной железы в рацион питания можно включать до 400-500 г углеводов в сутки. С целью адекватной функциональной адаптации органов пищеварения к выпадению функций желчного пузыря целесообразно как можно более раннее (в зависимости от сопутствующих заболеваний) расширение диеты. Основные принципы консервативной терапии заключаются в восстановлении нормального биохимического состава желчи, оттока желчи и панкреатического секрета в двенадцатиперстную кишку, а также в лечении заболеваний, ассоциированных с патологией билиарного тракта.
При наличии хронической билиарной недостаточности необходима заместительная терапия препаратами урсодеоксихолевой кислоты (УДХК). Наш опыт показывает, что применение УДХК в средней суточной дозе 10-15 мг на 1 кг массы тела эффективно уменьшает степень билиарной недостаточности и выраженность дисхолии. Доза и длительность лечения УДХК определяются степенью билиарной недостаточности и динамикой изменения холатохолестеринового коэффициента на фоне терапии.
Для обеспечения адекватного желчеоттока показаны миотропные спазмолитики: гимекромон – 200-400 мг 3 раза в день или мебеверина гидрохлорид по 200 мг 2 раза в день, или пинаверия бромид по 50-100 мг 3 раза в день в течение 2-4 нед.
Препараты указанной группы оказывают в основном спазмолитический эффект и не влияют на характер патологических изменений в печени. В связи с этим заслуживает внимания гепабене – комбинированный препарат растительного происхождения, состоящий из экстракта дымянки аптечной и экстракта расторопши пятнистой.
Экстракт дымянки лекарственной (Fumaria officinalis), содержащий алкалоид фумарин, оказывает желчегонное действие, обладает спазмолитическим действием, понижает тонус сфинктера Одди, облегчая поступление желчи в кишечник.
Экстракт плодов расторопши пятнистой (Fructus Silybi mariani) содержит силимарин – группу флавоноидных соединений, включающую изомеры: силибинин, силидианин и силикристин. Силимарин оказывает гепатопротективное действие: связывает свободные радикалы в ткани печени, обладает антиоксидантной мембраностабилизирующей активностью, стимулирует синтез белка, способствует регенерации гепатоцитов, нормализуя, таким образом, различные функции печени при острых и хронических заболеваниях печени. На фоне терапии гепабене стабилизируется биохимический состав желчи, уменьшается индекс насыщения холестерином пузырной желчи . Двойной механизм действия гепабене (спазмолитический и гепатопротективный) делают его одним из препаратов выбора у больных ПХЭС. Назначают гепабене по 1-2 капсулы 3 раза в день, курс лечения – 1-3 мес.
При наличии синдрома избыточного бактериального роста назначают антибактериальные препараты – ко-тримоксазол, интетрикс, фуразолидон, нифуроксацид, ципрофлоксацин, эритромицин, кларитромицин, которые применяют в общепринятых дозах. Курс лечения – 7 дней. При необходимости проводится несколько курсов антибактериальной терапии со сменой препаратов в очередном курсе. Весьма перспективными в лечении СИБР могут стать не всасывающиеся антибиотики. Первые опыты применения рифаксимина в клинике показывают, что препарат нормализует бактериальную микрофлору, уменьшает симптомы дуоденальной гипертензии, что имеет важное значение и у больных ПХЭС. После антибактериального курса назначают пробиотики (бифиформ, бифидумбактерин, споробактерин и др.), пребиотики – хилак-форте, который нормализует кишечную микрофлору, стимулирует регенерацию повреждённых деконьюгированными желчными кислотами эпителиоцитов кишечной стенки.
Для связывания избытка желчных и других органических кислот, особенно при наличии холагенной диареи, показано применение алюминий-содержащих антацидов по 10-15 мл (1 пакетик) 3-4 раза в день через 1-2 ч после еды в течение 7-14 дней. По показаниям возможно применение ферментных препаратов (панкреатин и др.).
В позднем послеоперационном периоде может возникнуть ряд осложнений, требующих проведения повторных операций. Рецидив камней встречается достаточно редко и возникает при условии существования причин, способствующих их формированию (нарушение оттока желчи и секреция литогенной желчи). Камни общего желчного протока удаляют с помощью баллонной дилатации, папиллотомии или папиллосфинктеротомии. В ряде случаев эти операции сочетают с контактной литотрипсией. Рецидив стриктур, по данным Э.И. Гальперина , является наиболее частым осложнением и составляет 10-30 % после операций на рубцово-изменённых желчных протоках. Рестенозы большого дуоденального сосочка развиваются и после папиллосфинктеротомии, в связи с чем может возникнуть вопрос о целесообразности наложения холедоходуоденоанастомоза.
Профилактика
Мероприятия по профилактике заключаются в комплексном обследовании больных в процессе подготовки к операции с целью выявления и своевременного лечения в первую очередь заболеваний гепатопанкреатодуоденальной зоны. Технически грамотно и в полном объёме выполненная операция, при необходимости с применением интраоперационных диагностических методик, важна и направлена на профилактику послеоперационных осложнений и постхолецистэктомического синдрома в частности. Одним из основных условий профилактики ПХЭС является своевременно выполненное хирургическое вмешательство до развития осложнений заболевания, а также в необходимом объёме проведённая предоперационная подготовка с целью коррекции выявленных нарушений. Однако высокая оперативная активность при ЖКБ связана с высокими экономическими затратами здравоохранения (таблица). В связи с этим наиболее эффективным путём профилактики холелитиаза и, как следствие ПХЭС, является выявление и лечение больных ЖКБ на ранних (предкаменных стадиях). С этой целью Центральным НИИ гастроэнтерологии была разработана современная клиническая классификация ЖКБ:
I стадия – начальная или предкаменная:
А. Густая неоднородная желчь
Б. Формирование билиарного сладжа • с наличием микролитов;
• с наличием замазкообразной желчи;
• сочетание замазкообразной желчи с микролитами.
II стадия – формирование желчных камней:
А. По локализации: • в желчном пузыре (холецистолитиаз);
• в общем желчном протоке (холедохолитиаз);
• в печёночных протоках.
Б. По количеству:
• одиночные;
• множественные.
В. По составу:
• холестериновые;
• билирубиновые;
• смешанные. Г. По клиническому течению: а) латентное течение;
б) с наличием клинических симптомов: • болевая форма с типичными желчными коликами;
• диспепсическая форма;
• под маской других заболеваний.
III стадия – калькулезного холецистита.
IVстадия – осложнений.
Классификация обсуждена и рекомендована к применению в клинической практике III съездом НОГР (2003 г., опубликована в Тер. архиве № 2, 2004).
Как показали исследования применение коротких курсов терапии, направленной на ликвидацию билиарных дисфункций и восстановление нормального биохимического состава желчи может быть эффективным средством первичной профилактики холелитиаза.
![]()
Вопрос-ответ / Список вопросов
Вопрос: У меня болезнь: рефлюкс-эзофагит, недостаточность пилорического клапана. Симптомы: отрыжка после еды, изжога с утра маленькая,ощущение сытости после небольшого приёма пищи.Понизители кислотности не помогают, делают еще хуже.
Сейчас лечусь иглотерапией, газов стало меньше, остальные симптомы почти исчезли. Газы перешли в правую часть желудка.
Вопрос в том, стоит ли продолжать лечение?
Я уже лечу полтора месяца, стало на 50% легче, но стоит на месте, лучше не становится.
Лечит ли акупунктура такой вид заболевания, или даёт только облегчение?
Может лучше сделать операцию?
Ответ (15.06.2008): К сожалению, Вы даёте мало информации.
«Понизители кислотности не помогают, делают еще хуже.» какой …
Вопрос: У меня такой вопрос. Я в течении последних пяти лет страдаю болями в сердце, экстрасистолами, слабостью, нечеткой походкой, закладыванием ушей, дурнотой. Все эти симптомы увеличиваются при нервных срывах,принятии пиши и передвижениях на транспорте. Неоднакратно проходил обследование у различных врачей: кардиолога, невропатолога, офтальмолога, психолога, лечился в стационаре у невропатолога. Делали кучу анализов, исследований УЗИ, МРТ головы и шейного отдела позвоночника: все практически в норме. И вот пол-года назад гастроэнтеролог назначил исследование пищевода и выявилась ГПОД, могут ли из-за неё быть такие симтомы. Назначил париэт, но особого результате не дало, сказал пей и все пройдет. Хотелось бы узнать, что сделать, говорят операция все исправит, так ли это. А то эта гадость за пять лет совсем измучила. Спасибо за ответ.
Ответ (15.06.2008): Считаю, что вряд ли наличие ГПОД вызывает подобные проявления. Слабость, нечеткую походку и …
Вопрос: По заключению гастроскопии: Грыжа ПОД, катаральный эзофагит, эрозивный фундальный гастрит. Назначен курс париета.
Вопрос: насколько серьёзно наличие грыжи, смогу ли я прожить с ней без всяких операций. Можно ли делать физические упражнения для укрепления мышц спины (проблемы с позвоночником)?
Ответ (15.06.2008): Как правило, в подавляющем большинстве случае, грыжи ПОД не требуют выполнения оперативного пособия. …
Вопрос: Выполнено удаление желчного пузыря, какие продукты можно кушать?
Ответ (15.06.2008): Лечебное питание должно предупреждать застой желчи в желчевыводящих путях, обеспечивать профилактику образования …
Вопрос: Здравствуйте! Недавно пролечилась Амепрозолом от язвы 12-типерстной кишки. Какие могут быть реакции организма на этот препарат? Ощущается жжение (+ покраснение, шелушение кожи) на слизистых и во время мочеиспускания.
Ответ (10.06.2008): Аллергические реакции могут быть на любой препарат и в любом виде. Если их возникновение Вы чётко …
Вопрос: За сколько часов нельзя есть и пить перед ФГДС?
Ответ (10.06.2008): Всё зависит от индивидуальных особеностей каждого человека. Но обычно 4-5 часов. Как правило ФГДС …
Вопрос: Здравствуйте,доктор! Нужно ли принимать какие-либо препараты, травы после лапароскопического удаления жп (10 дней назад), дабы помочь перестроиться организму работать без жп? 12 камней. Сейчас состояние удовл., других заболеваний жкт не выявлено. Спасибо.
Ответ (10.06.2008): Рекомендую периодически принимать желчегонные травы и сборы для профилактики камнеобразования в протоках. Если нет …
Вопрос: Здравствуйте, дорогие специалисты. Моему ребенку 16 лет. На днях ставили ему диагноз, полип желчного пузыря, но у него имеется еще язва двенадцатиперстной кишки. Ответьте, пожалуйста, чем чревато удаление желчного пузыря и нет ли лечения препаратами или травами, чтобы избежать операции? Но нам еще не предлагали, я читала,что можно лечить народными средствами-чистотелом (трава). На сколько процентов это возможно? Ведь сами понимаете, моему сыну только 16 лет вся жизнь впереди. Как мне помочь, что мне делать, какими способами вылечить, но только без удаления желчного пузыря. Заранее благодарна. Жду с нетерпением ответа. С уважением, Сюзи.
Ответ (10.06.2008): Рекомендую уточнить сначала, полип ли это. Может быть это холестероз желчного пузыря, то есть начальное проявление желчно-каменной болезни и …
Вопрос: Здравствуйте, моему мужу 30 лет. Как он говорит — он с детства «мучается с животом». Раз в 1-2 месяца у него неукротимая рвота, понос и всё это продолжается по 2-3 дня. Год назад он всё-таки пошел в больницу. По результатам гастроскопии и рентгеноскопии ему поставили диагноз массивная ГПОД, гастрит, рефлюкс-эзофагит, синдром … (не помню точно как называется, но смысл в том, что это надрывы слизистой пищевода). Терапевт сказал, что надо срочно делать операцию, так как во время приступа рвоты может произойти отрыв грыжи и пищевода от желудка (так ли это?), послал к торакальному хирургу, но тот сказал, что операцию делать не надо. Послал к гастроэнтерологу, тот сказал пропить курс Омеза и соблюдать диету. Но с каждым приступом мужу тановится всё хуже и хуже. На прошлой неделе его рвало, рваться нечем, а всё равно рвет. Церукал на него действует только через 3-4 часа (до этого он просто вырывает таблетки). Начало уже с кровью рвать. Что нам делать? Необходима ли операция или возможно какое-нибудь медикаментозное лечение? Проводят ли в Туле такие операции? Заранее спасибо за ответ.
Ответ (10.06.2008): ГПОД, гастрит, рефлюкс-эзофагит вряд ли будут причиной неукротимой рвоты. Синдром Меллори-Вейса это …
Вопрос: Во рту сильный, постоянный, горько-солёный вкус, жжение, повышеное слюноотделение.
Ответ (10.06.2008): Скорее всего горечь во рту бывает за счёт патологии желчевыводящих путей. Для уточнения причины рекомендую …
Вопрос: Добрый день! ГЭРБ, ГПОД. Лекарственное лечение дает облегчение ненадолго , в настоящее время принимаю 2 таблетки Париета 20 мг в день , только так удалось избавиться от обострения эрозивного рефлюкс-эзофагита , на последнем ФГДС нет эрозий в пищеводе. Одной таблетки мало. Постоянно отрыжка, периодически трудности при глотании, ощущение тяжести ,отдающее в область между лопаток. Если не принимать таблетки, то, кроме изжоги и болей в пищеводе, добавляется мучительный кашель. В таком режиме на лекарствах уже более 2-х лет . Хочу сделать операцию . Посоветуйте ,операция поможет ? Как долго длится восстановительный период после операции? Спасибо.
Ответ (25.05.2008): Думаю, что постоянно принимать препараты, относящиеся к ингибиторам протонной помпы не стоит. В таких случаях, для многолетнего приёма, …
Вопрос: После опперации лапороскопии желчного пузыря как нужно питаться и принимать препараты поддерживающие печень?
Ответ (25.05.2008): Лечебное питание должно предупреждать застой желчи в желчевыводящих путях, обеспечивать профилактику образования …
Вопрос: Добрый вечер. Три года назад удалили желчный (камни, приступ). Через три месяца после операции начались боли в левом подреберье. Болит практически постоянно только с разной силой. Рекомендации врачей не помогают, спасает лишь баралгин внутримышечно. На обследовании желудка-гастрит, дуоденит, рефлюкс. Причину всего этого не понимаю.. Может что подскажите, буду очень благодарна.
Ответ (25.05.2008): Скорее всего у Вас развился постхолецистэктомический синдром в виде хронического панкреатита. Обострения этого …
Вопрос: У меня к вам такой вопрос..Ходила недавно на УЗИ и там обнаружили камни в желчном пузыре, причем он заполнен весь. Самый большой 22мм, и сказали, что срочно надо делать операцию. Но меня он не беспокоит. Стоит ли «ложится под нож»? Можно ли удалить его лапароскопическим путем? И какой наркоз делается при лапароскопии? заранее спасибо:-)!
Ответ (19.05.2008): Ващ желчный пузырь придётся удалять всё равно, рано или поздно. Лучше это сделать в «холодном» …
Вопрос: У меня камень в желчном пузыре 6 мм и больная печень.Можно ли удалить его без операции?
Ответ (19.05.2008): Удалить желчный пузырь можно только оперативно. Можно попробовать растворить камни в желчном пузыре медикаментозно, но …
Вопрос: Какие осложнения чаще всего возникают после операции грыж диафрагмы отверстия пищевода?
Ответ (19.05.2008): Чаще всего бывают болевые ощущения при глотании и изжога.
Вопрос: Здравствуйте. Уже в течении 2 лет часто отхаркиваюсь странной слизью, много раз на дню, особенно после еды — в частности быстрая реакция после жирного и сладкого, хотя стараюсь себя в этом ограничивать. При этом насморка почти не наблюдается. А в последнее время замечаю различного рода колики справой стороны живота и груди — периодически. Подскажите, из-за чего эта слизь и может ли это быть связано с коликами.
Ответ (19.05.2008): Скорее всего Ваша слизь происходит не из органов желудочно-кишечного тракта, а из дыхательных путей трахеи и бронхов. …
Вопрос: Скажите пожалуйста, можно ли после удаления желчного пузыря принимать Эссенциале?
Ответ (11.05.2008): Можно, ведь эссенциале воздействует на печень, а не на желчевыводящие пути.
| » Предыдущие 10 | 1 | 2 | 3 | 4 | 5 | 6 | Следующие 10 « |
Задайте вопрос
Искусственные органы медленно, но верно перемещаются из области научной фантастики в сферу практической медицины. В обозримом будущем большинство составных частей человеческого организма, вполне возможно, будут иметь искусственное происхождение. У пластических хирургов может появиться много почти коллег — специалистов по ремонту и обслуживанию человеческих тел.
ЯКОВ МОТЫЛЬКОВ
Найдите минимум отличий
Сразу же следует уточнить, что в статье речь пойдет не о набитых электроникой и густо обвязанных проводами больших железных ящиках (именно так выглядит некогда очень популярный в среде генсеков ЦК КПСС аппарат «искусственная почка»).
Для разделения понятий можно позаимствовать удобный и легкопроизносимый термин у фантастов. Артифорг (Artificial Organ) — искусственный орган человеческого тела должен размещаться внутри этого тела, соответствуя по размерам своему прототипу. Железный шкаф «почка», плюс железный шкаф «легкие», плюс другие железные шкафы в сумме дадут не гомо сапиенса, а киборга, немобильного и плохо приспособленного к реальной жизни.
Вместо проводов должны использоваться кровеносные сосуды, а материал, из которого изготовлено новое сердце (печень, селезенка, желудок и т. д.), не должен отторгаться организмом. На начальном этапе органы будут производиться из различных пластиков или же прошедших специальную обработку органов животных. Затем им на смену должны прийти технологии выращивания новых органов (в организме самого пациента, в лабораторной пробирке, в организме клонированного животного). Ведутся исследования и в направлении регенерации. Если ящерицы способны отращивать потерянные хвосты, может, и человек сможет сделать нечто похожее? При наличии квалифицированной помощи, конечно.
С точки зрения финансовой ситуация на рынке артифоргов с самого его возникновения будет такова, о какой практически в любом другом виде бизнеса продавцы не могут и мечтать. Спрос будет многократно перекрывать предложение. Покупателям остается утешаться мыслью о том, как дорого стоит их жизнь. Примерное представление о ценах можно составить, если учесть, что кохлеарный имплантат (позволяющий глухому слышать) стоит в России вместе с установкой от 1 млн руб., при том что речь идет об относительно несложном в изготовлении и не самом жизненно важном органе — в сравнении, скажем, с печенью или сердцем.
Из положительных моментов следует отметить, что артифорги могут положить конец незаконным операциям с донорскими органами. Впрочем, это будет тоже зависеть от цены.
Главное — не терять голову
Начнем с грустного. Хотя современная наука добилась определенных успехов в области создания искусственного интеллекта, возможность разработки имплантата человеческого мозга пока даже не обсуждается. Рано.
Современная медицина может похвастаться лишь искусственным костным мозгом, да и то не самым высококачественным. Группа исследователей во главе с профессором Николасом Котовым из Университета Мичигана в 2008 году представила созданный ею полимер, повторяющий по структуре человеческий костный мозг. Профессор Котов отвергает возможность вживления этого мозга людям, он пока будет существовать исключительно в пробирке и служить для испытаний новых лекарственных средств.
Четыре года до сердца
Сердце, пожалуй, одна из самых важных деталей человеческого организма после головного мозга. Первые попытки создания искусственного сердца относят чуть ли не к 1812 году. В середине прошлого века на этом направлении уже наметился заметный прогресс, лабораторные собачки и телята после каждой новой операции по вживлению искусственного сердца жили все дольше, однако это время все равно измерялось часами. В последние годы очередь дошла и до людей.
В 2006 году в одной из детских клиник Канады 15-летней пациентке был установлен сердечный имплантат (не на замену, а в дополнение к ее собственному сердцу), который давал девочке казавшийся не очень высоким шанс дожить до момента, когда удастся найти донорское сердце для операции. Донор не понадобился. Пять месяцев спустя деятельность сердца восстановилась, имплантат был удален.
В 2008 году кардиохирург-трансплантолог из Франции Ален Карпентье заявил, что полный имплантат человеческого сердца будет готов к клиническим испытаниям в 2011 году, а в 2013 году можно будет ожидать первые операции. Над подобными проектами параллельно работает несколько групп исследователей в разных странах.
24 июня 2009 года в больнице Университета Роберта Вуда Джонсона (штат Нью-Джерси, США) прошла первая операция по установке пациенту официально утвержденного к применению сердечного имплантата AbioCor (с удалением родного сердца). В ближайшие годы должно быть установлено несколько сотен, а может, и тысяч таких искусственных сердец. Операция может быть проведена только на пациенте, которому без замены сердца осталось жить не более месяца. Трансплантат должен подарить дополнительные год-два жизни. Разумеется, с развитием технологии оба срока будут удлиняться.
Одна из решенных не до конца проблем на пути массового производства сердечных трансплантатов состоит в том, что искусственное сердце нуждается в источнике питания, заряд которого следует контролировать (наверное, нет нужды объяснять, что будет, если источник питания разрядится). Для простоты такого контроля «батарейка» должна быть закреплена на теле снаружи, а провода от нее — проходить внутри организма.
Если сердце может быть сделано человеком, почему бы ему не перегонять искусственную кровь по искусственным венам? О полной замене крови, правда, пока речь не идет. Но многочисленные исследователи уже активно занимаются созданием жидкостей, которые можно добавлять в кровь с разными целями. Самые простые заменители, уже существующие, не очень хороши. В случае большой кровопотери (например, при катастрофах) и при отсутствии необходимого количества донорской крови их можно залить в кровеносную систему, увеличив объем жидкости в ней до нормального уровня. Правда, при этом упадет уровень гемоглобина. Двух-, трех-, а в отдельных случаях и семикратное падение этого уровня человеческий организм может пережить. Но время, чтобы дождаться неотложной медицинской помощи, выигрывается.
Следующее поколение искусственной крови — искусственная кровь, способная доставлять внутренним органам кислород.
Из достижений в области кровообращения современная медицина может похвастаться имплантацией искусственного заменителя одного из важнейших органов (на мой субъективный взгляд) — пещеристого тела полового члена. Сексуального равноправия ради хочу отметить, что создание искусственных яичников уже не за горами. Исследователи из английского Университета Брауна утверждают, что таковые появятся уже скоро.
Глаз или видеть
По поводу искусственных глаз есть две новости — плохая и хорошая. Плохая состоит в том, что ни один нормально действующий протез, дающий человеку возможность видеть, не выглядит как глаз. Если слепой, слабовидящий, потерявший глаз или сильно его повредивший человек способен примириться с тем, что будет внешне слегка напоминать Терминатора, то вот хорошая новость: жуткий на вид искусственный глаз будет работать. Не то чтобы им можно будет рассматривать почтовую марку в лупу или хотя бы любоваться картинами — нет, такое пока невозможно. Но уровень освещенности, примерные цвета, общие очертания предметов — это искусственный глаз «увидеть» может.
Проектов по созданию искусственных органов зрения в мире немало. Этим занимаются в тюбингенской университетской офтальмологической больнице, в престижном Массачусетском технологическом институте, в не менее престижном Стэнфорде, в Иллинойском технологическом институте, в университетах Юты и Чикаго, Политехнической школе в Монреале, в Японии и Австралии. В ЕС действует специальная программа исследований в этой сфере.
При этом все разработчики искусственных органов зрения идут примерно одним путем. Искусственный глаз — это цифровая видеокамера; снимаемый с нее сигнал используется для стимуляции сетчатки глаза и (или) оптического нерва напрямую. Развитию этого направления медицины невольно способствует тот факт, что исследованиями в области цифрового видео занимаются суперкорпорации, выпускающие бытовую и компьютерную технику.
Если предположить, что путь создания искусственных органов зрения будет похож на историю развития бытовых фотоаппаратов, а займет при этом как минимум вдвое меньше времени, то вполне возможно, что уже в нынешнем веке будет создан искусственный глаз, функционально полностью соответствующий живому.
Искусственные органы слуха до подобного «уровня натуральности» уже почти дошли. Маркетинговые материалы компаний, выпускающих «искусственные уши», обещают «музыкальное качество», но при этом скорее торопят события, чем обманывают. Людей, пользующихся искусственными органами слуха, в мире больше, чем пациентов со всеми остальными искусственными органами, вместе взятыми. За исключением, конечно, зубов. А к концу XXI века, вероятнее всего, глухим останется лишь тот, кто сам выразит желание быть таковым.
Вместе со словом «глухой» должны устареть также понятия «беспалый», «безрукий», «безногий». Искусственные конечности активно разрабатываются и производятся по всему миру. До идентичности искусственных и «родных» рук и ног сегодня дело еще не дошло, но бурный прогресс в этой области практически неизбежен.
Искусственная кожа и искусственные кости станут реальностью всего через несколько лет. Первую создают в Массачусетском технологическом институте, вторые — в Университете Макджилла в Монреале.
Плановая замена и капремонт
В деле создания искусственной печени медицина пока продвинулась недалеко (в сравнении с другими областями). Компания HepaLife ведет разработки искусственной печени PICM-19, которая должна будет не заменять, а лишь дополнять родную печень пациента, взяв на себя часть ее функций — в ожидании или нормализации работы родной печени, или донорской печени для пересадки.
О полной замене печени пока речь даже не идет. Специалисты по регенеративной медицине из Университета Ньюкасла полагают, что примерно в 2012 году появятся разработки, позволяющие «ремонтировать» больную печень за счет отдельных клеток, созданных искусственным путем.
Первые (внешние металлические, конечно) искусственные легкие были созданы еще в двадцатые годы XX века. Искусственные легкие сегодняшнего дня — отдельно стоящая машина. Но уже есть разработки этого органа, которые не нужно ставить отдельно, а можно удержать на весу в одной руке. Это искусственное легкое Novalung, выпускаемое одноименной компанией. Его имплантация пока, увы, невозможна: легкое придется «носить» на себе наподобие небольшого рюкзачка. Появление полнофункциональных искусственных легких, имплантируемых в тело, специалисты обещают уже в ближайшее время.
Созданием искусственной поджелудочной железы занимаются в целях борьбы с диабетом. Изучается возможность имплантации клеток, вырабатывающих инсулин, в больной орган. Альтернативное направление — более технологичное, предполагается создать искусственный орган, который в перспективе может даже превзойти тот, который дан человеку природой. Искусственная поджелудочная железа должна, как предполагается, отслеживать изменения уровня инсулина в организме и вырабатывать необходимое количество в соответствии с полученными данными. Пока же в Медицинской школе Монпелье идут клинические испытания искусственных поджелудочных желез, которые представляют собой что-то вроде вживленного в организм миниатюрного робота-сиделки. Артифорг контролирует уровень инсулина и, если тот снижается, фактически делает укол.
Уже три года прошло с момента первой в мире операции по имплантации замены желчного пузыря. На этом направлении победу одержали специалисты по биотехнологиям. Желчные пузыри выращивают из клеток, а не собирают на станке. Тогда, в 2006 году, искусственными желчными пузырями успешно обзавелись семеро человек. Новые органы были созданы с использованием родных клеток пациентов.
Вполне возможно, что по схожим технологиям могут быть созданы искусственная печень и искусственные почки, а может быть — и искусственное сердце.
Слову «бесплодная» придется также отправиться в архив. Однако искусственная матка, в отличие от других искусственных органов, должна не вживляться в тело, а находиться вне него. Человеческий эмбрион будет развиваться в специальной камере, поневоле заставляющей вспомнить книгу «Дивный новый мир» и фильм «Секс-миссия». И произойдет это, как утверждает занимающийся разработкой искусственной матки доктор Лю Хун Чин из Центра репродуктивной медицины и борьбы с бесплодием Корнуэльского университета, в самом ближайшем будущем.